Manieren om interne energie te veranderen. Interne lichaamsenergie
Voor oplossingen praktische problemen Het is niet de interne energie zelf die een belangrijke rol speelt, maar de verandering ervan Δ U = U 2 - U 1. Wijziging interne energie berekend op basis van de wetten van behoud van energie.
De interne energie van een lichaam kan op twee manieren veranderen:
1. Na voltooiing mechanisch werk .
a) Als een externe kracht vervorming van een lichaam veroorzaakt, veranderen de afstanden tussen de deeltjes waaruit het bestaat, en daarom verandert de potentiële energie van interactie van deeltjes. Tijdens inelastische vervormingen verandert bovendien de lichaamstemperatuur, d.w.z. de kinetische energie van thermische beweging van deeltjes verandert. Maar wanneer een lichaam vervormd is, wordt er arbeid verricht, wat een maatstaf is voor de verandering in de interne energie van het lichaam.
b) De interne energie van een lichaam verandert ook tijdens de inelastische botsing met een ander lichaam. Zoals we eerder zagen, neemt tijdens een inelastische botsing van lichamen hun kinetische energie af, het verandert in interne energie (als je bijvoorbeeld meerdere keren met een hamer op een draad slaat die op een aambeeld ligt, zal de draad opwarmen). De maatstaf voor de verandering in de kinetische energie van een lichaam is, volgens de kinetische energiestelling, het werk van de werkende krachten. Dit werk kan ook dienen als een maatstaf voor veranderingen in interne energie.
c) Een verandering in de interne energie van een lichaam vindt plaats onder invloed van wrijving, aangezien wrijving, zoals uit ervaring bekend is, altijd gepaard gaat met een verandering in de temperatuur van wrijvende lichamen. De arbeid die door de wrijvingskracht wordt verricht, kan dienen als maatstaf voor de verandering in interne energie.
2. Gebruik warmte uitwisseling. Als een lichaam bijvoorbeeld in de vlam van een brander wordt geplaatst, zal de temperatuur ervan veranderen en daarom zal de interne energie ook veranderen. Hier werd echter geen werk verricht, omdat er geen zichtbare beweging was van het lichaam zelf of van de delen ervan.
Een verandering in de interne energie van een systeem zonder werk te doen, wordt genoemd warmte uitwisseling(warmteoverdracht).
Er zijn drie soorten warmteoverdracht: geleiding, convectie en straling.
A) Warmtegeleiding is het proces van warmte-uitwisseling tussen lichamen (of delen van een lichaam) tijdens hun directe contact, veroorzaakt door de thermische chaotische beweging van lichaamsdeeltjes. Hoe hoger de temperatuur, hoe groter de amplitude van de trillingen van de moleculen van een vast lichaam. De thermische geleidbaarheid van gassen is te danken aan de uitwisseling van energie tussen gasmoleculen tijdens hun botsingen. Bij vloeistoffen werken beide mechanismen. De thermische geleidbaarheid van een stof is maximaal in de vaste toestand en minimaal in de gasvormige toestand.
B) Convectie vertegenwoordigt warmteoverdracht door verwarmde vloeistof- of gasstromen van sommige delen van het volume dat ze innemen naar andere.
c) Warmte-uitwisseling bij straling op afstand via elektromagnetische golven.
Laten we de manieren om de interne energie te veranderen in meer detail bekijken.
Hoeveelheid warmte
Zoals bekend, op verschillende mechanische processen mechanische energieveranderingen W. Een maatstaf voor de verandering in mechanische energie is het werk van krachten die op het systeem worden uitgeoefend:
Tijdens de warmte-uitwisseling vindt er een verandering plaats in de interne energie van het lichaam. Een maatstaf voor de verandering in interne energie tijdens warmteoverdracht is de hoeveelheid warmte.
Hoeveelheid warmte is een maatstaf voor de verandering in interne energie tijdens warmteoverdracht.
Zowel de arbeid als de hoeveelheid warmte karakteriseren dus de verandering in energie, maar zijn niet identiek aan interne energie. Ze karakteriseren niet de toestand van het systeem zelf (zoals interne energie doet), maar bepalen het proces van energietransitie van het ene type naar het andere (van het ene lichaam naar het andere) wanneer de toestand verandert, en zijn in belangrijke mate afhankelijk van de aard van het proces.
Het belangrijkste verschil tussen werk en warmte is dat
§ werk karakteriseert het proces van het veranderen van de interne energie van een systeem, vergezeld van de transformatie van energie van het ene type naar het andere (van mechanisch naar intern);
§ de hoeveelheid warmte karakteriseert het proces van overdracht van interne energie van het ene lichaam naar het andere (van meer verwarmd naar minder verwarmd), dat niet gepaard gaat met energietransformaties.
§ Warmte capaciteit, de hoeveelheid warmte die nodig is om de temperatuur met 1°C te veranderen. Volgens een strengere definitie warmte capaciteit- thermodynamische grootheid bepaald door de uitdrukking:
§ waarbij Δ Q- de hoeveelheid warmte die aan het systeem wordt doorgegeven en waardoor de temperatuur ervan verandert door Delta T; Eindige verschilverhouding Δ Q/ΔТ wordt gemiddeld genoemd warmte capaciteit, de verhouding van oneindig kleine hoeveelheden d Q/dT- WAAR warmte capaciteit. Sinds d Q is dus geen volledig verschil in de staatsfunctie warmte capaciteit hangt af van het overgangspad tussen twee toestanden van het systeem. Onderscheiden warmte capaciteit systeem als geheel (J/K), specifiek warmte capaciteit[J/(g K)], molair warmte capaciteit[J/(mol K)]. Alle onderstaande formules gebruiken molaire hoeveelheden warmte capaciteit.
Vraag 32:
Interne energie kan op twee manieren worden veranderd.
De hoeveelheid warmte (Q) is de verandering in de interne energie van een lichaam die optreedt als gevolg van warmteoverdracht.
De hoeveelheid warmte wordt gemeten in SI-eenheden in joule.
[Q] = 1J.
De soortelijke warmtecapaciteit van een stof laat zien hoeveel warmte er nodig is om de temperatuur van een eenheidsmassa te veranderen van deze stof met 1°C.
Eenheid specifieke warmte capaciteit in het SI-systeem:
[c] = 1 J/kg °C.
Vraag 33:
33
De eerste wet van de thermodynamica is de hoeveelheid warmte die een systeem ontvangt om zijn interne energie te veranderen en aan externe lichamen te werken. dQ=dU+dA, waarbij dQ de elementaire hoeveelheid warmte is, dA de elementaire arbeid is, en dU de toename van de interne energie is. Toepassing van de eerste wet van de thermodynamica op isoprocessen
Onder de evenwichtsprocessen die optreden bij thermodynamische systemen vallen de volgende op: isoprocessen, waarbij een van de belangrijkste toestandsparameters constant blijft.
Isochoor proces (V=constant). Diagram van dit proces (isochoor) in coördinaten R, V wordt weergegeven als een rechte lijn evenwijdig aan de ordinaatas (Fig. 81), waar het proces plaatsvindt 1-2
er is isochorische verwarming, en 1
-3 -
isochore koeling. Bij een isochoor proces werkt het gas niet op externe lichamen.  Isotherm proces (T=const). Zoals reeds aangegeven in § 41, wordt het isotherme proces beschreven door de wet van Boyle-Mariotte
Isotherm proces (T=const). Zoals reeds aangegeven in § 41, wordt het isotherme proces beschreven door de wet van Boyle-Mariotte
, om ervoor te zorgen dat de temperatuur niet daalt tijdens de gasexpansie, een hoeveelheid warmte gelijk aan extern werk extensies.
Vraag 34:
34 Adiabatisch is een proces waarbij er geen warmte-uitwisseling plaatsvindt ( dQ= 0)tussen het systeem en omgeving. Alle snelle processen kunnen worden geclassificeerd als adiabatische processen. Het voortplantingsproces van geluid in een medium kan bijvoorbeeld als een adiabatisch proces worden beschouwd, omdat de voortplantingssnelheid van een geluidsgolf zo hoog is dat de uitwisseling van energie tussen de golf en het medium geen tijd heeft om plaats te vinden. Adiabatische processen worden gebruikt in verbrandingsmotoren (expansie en compressie van het brandbare mengsel in de cilinders), in koeleenheden enz.
Van de eerste wet van de thermodynamica ( dQ= D U+dA) voor een adiabatisch proces volgt dit ![]() p /С V =γ , vinden we
p /С V =γ , vinden we
Door de vergelijking van p 1 naar p 2 en dienovereenkomstig van V 1 naar V 2 te integreren en te potentiëren, komen we tot de uitdrukking
Omdat toestanden 1 en 2 willekeurig worden gekozen, kunnen we schrijven
De interne energie van een lichaam is niet een soort constante waarde. Het kan in hetzelfde lichaam veranderen. Naarmate de temperatuur stijgt, neemt de interne energie van een lichaam toe omdat deze toeneemt gemiddelde snelheid moleculaire bewegingen. Bijgevolg neemt de kinetische energie van de moleculen van dit lichaam toe. Naarmate de temperatuur daalt, neemt daarentegen de interne energie van het lichaam af. De interne energie van een lichaam verandert dus wanneer de bewegingssnelheid van de moleculen verandert. Laten we proberen erachter te komen hoe we de bewegingssnelheid van moleculen kunnen verhogen of verlagen.
Om dit te doen, doen we het volgende experiment. Laten we een dunwandige koperen buis aan een standaard bevestigen (Fig. 4). Giet wat ether in het buisje en sluit het af met een stop. Dan zullen we de buis met een touw vastbinden en hem snel in de ene richting bewegen, en dan in de andere. Na enige tijd zal de ether koken en zal de stoom de plug naar buiten duwen. De ervaring leert dat de interne energie van de ether is toegenomen: deze is immers opgewarmd en zelfs gekookt. De toename van de interne energie vond plaats als gevolg van het werk dat werd gedaan bij het wrijven van de buis met een touw. Verwarming van lichamen vindt ook plaats tijdens botsingen , verlenging en buiging, dat wil zeggen tijdens vervorming. De interne energie van het lichaam in alle bovenstaande voorbeelden neemt toe. Vandaar, De interne energie van een lichaam kan worden vergroot door werk aan het lichaam te doen. Als het werk door het lichaam zelf wordt gedaan, neemt de interne energie af. Laten we het volgende experiment doen. We pompen lucht in een dikwandig glazen vat, afgesloten met een stop, via een speciaal gat erin (fig. 5). Na enige tijd zal de kurk uit het vat springen. Op het moment dat de kurk uit de container springt, ontstaat er mist. Het uiterlijk betekent dat de lucht in het vat kouder is geworden. De perslucht in het vat, die de plug naar buiten duwt, werkt wel. Hij doet dit werk ten koste van zijn interne energie, die afneemt. Je kunt de afname van de interne energie beoordelen door de lucht in het vat af te koelen. De interne energie van een lichaam kan dus worden veranderd door arbeid te verrichten.
De interne energie van het lichaam kan op een andere manier worden veranderd, zonder arbeid te verrichten. Water kookt bijvoorbeeld in een ketel die op het fornuis staat. De lucht en verschillende voorwerpen in de kamer worden door de radiator verwarmd centrale verwarming. In deze gevallen neemt de interne energie toe naarmate de lichaamstemperatuur stijgt. Maar het werk is niet gedaan. Dit betekent dat een verandering in interne energie niet alleen als gevolg van werk kan optreden.
De interne energie van lichamen kan worden veranderd door warmteoverdracht. Het proces van het veranderen van interne energie zonder werk aan het lichaam of het lichaam zelf te doen, wordt warmteoverdracht genoemd. Warmteoverdracht vindt altijd in een bepaalde richting plaats: van lichamen met een hogere temperatuur naar lichamen met een lagere temperatuur. Wanneer de lichaamstemperatuur gelijk is, stopt de warmteoverdracht.
De interne energie van een lichaam kan op twee manieren worden veranderd: door mechanisch werk uit te voeren of door warmteoverdracht. Warmteoverdracht kan op zijn beurt op drie manieren worden uitgevoerd: 1) thermische geleidbaarheid; 2) convectie; 3) straling.















 Terug vooruit
Terug vooruit
Aandacht! Diavoorbeelden zijn alleen voor informatieve doeleinden en vertegenwoordigen mogelijk niet alle functies van de presentatie. Als u geïnteresseerd bent in dit werk, download dan de volledige versie.
Lesdoelen:
- ontwikkeling van interesses en capaciteiten van studenten op basis van de overdracht van kennis en ervaring met cognitieve en creatieve activiteiten;
- het inzicht van studenten in belangrijke concepten als energie, interne energie, warmteoverdracht en de typen daarvan: thermische geleidbaarheid, straling, convectie;
- het ontwikkelen van de ideeën van leerlingen over de fundamentele natuurwetten aan de hand van het voorbeeld van de wet van behoud van energie.
Taken:
- studenten verwerven kennis over interne energie, manieren om deze te veranderen, bekendheid met de termen: warmteoverdracht, thermische geleidbaarheid, straling;
- het ontwikkelen van bij studenten het vermogen om natuurlijke verschijnselen te observeren, gedrag te vertonen experimentele onderzoeken, conclusies trekken;
- de beheersing van studenten van algemene wetenschappelijke concepten als een natuurlijk fenomeen, een empirisch vastgesteld feit, het resultaat van een experiment.
Lestype: gecombineerd.
Demo's:
- transformatie van mechanische energie (aan de hand van het voorbeeld van de beweging van een rubberen bal en de slinger van Maxwell);
- transformatie van mechanische energie in interne energie (met behulp van het voorbeeld van een loden bal die op een loden plaat valt);
- verandering in interne energie volgens figuren 4 en 5 van het leerboek (Perishkin A.V. Physics-8), het verwarmen van een munt in een kaarsvlam en bij het wrijven tegen een houten liniaal, het verwarmen van lood met hamerslagen;
- experimenten volgens figuur 6-9 in het leerboek (Peryshkin A.V. Physics-8);
- experimenten op Fig. 10.11 in het leerboek (Peryshkin A.V. Physics-8)
- observatie van convectie in gassen aan de hand van het voorbeeld van het observeren van convectiestromen van een brandende kaars in projectie op een verlicht scherm;
- demonstratie van lampen die gebruik maken van het fenomeen convectie;
- het verwarmen van de lucht in de warmteontvanger door straling;
- demonstratie van het absorptievermogen van verschillende stoffen.
Tijdens de lessen
Opmerking:
De materialen die in deze presentatie worden gepresenteerd omvatten verschillende onderwerpen die belangrijk zijn voor verdere studie van thermische verschijnselen en zijn ontworpen voor gebruik in verschillende lessen en bij het uitleggen nieuw onderwerp, zowel tijdens de algemene herhaling in het 8e leerjaar als bij het studeren van moleculaire fysica in het 10e leerjaar.
Het is raadzaam om de verworven kennis over dit onderwerp te consolideren met behulp van voorbeelden van problemen die voldoende vertegenwoordigd zijn in verzamelingen problemen in de natuurkunde:
- AV Peryshkin Verzameling van problemen in de natuurkunde, groep 7-9, red. "Examen" M., 2013.
- IN EN. Loekashik, E.V. Ivanova Verzameling van problemen in de natuurkunde, groep 7-9, red. "Verlichting" JSC "Moscow Textbooks", M., 2001.
- en anderen.
Daarom dit presentatie kan gedeeltelijk en (of) volledig in een les worden gebruikt, afhankelijk van de doelen en doelstellingen van deze les. Bijvoorbeeld bij het leren van nieuwe stof.
Uitleg nieuw materiaal:
Wanneer we beginnen met het formuleren van het concept van interne energie, is het noodzakelijk om leerlingen uit te nodigen om te onthouden wat ze weten over de mechanische energie van lichamen.
Vragen voor studenten:
- Wanneer wordt gezegd dat lichamen energie hebben?
- Welke soorten mechanische energie worden onderscheiden?
- Welke lichamen hebben kinetische energie en waar hangt deze van af?
- Waar hangt de potentiële energie van een lichaam van af?
- Geef voorbeelden van de transformatie van mechanische energie.
(Dia's 2-5)
Dia 2
Dia 3
Dia 4
Dia 5
De vorming van het concept van interne energie is gebaseerd op het idee van een schijnbare “schending” van de wet van behoud van energie wanneer een loden bal in botsing komt met een loden plaat.
Ervaring nr. 1. Impact van een loden bal op een loden plaat. Gebaseerd op de “overtreding” van de wet van behoud van energie en de studie van de toestand van de loden bal na de impact, concluderen ze dat alle lichamen energie hebben, die interne energie wordt genoemd (dia 6-8).
Dia 6
Dia 7
Dia 8
Vervolgens is het noodzakelijk om studenten het verschil uit te leggen tussen interne energie en mechanische energie van lichamen. Het is belangrijk om te concluderen dat de interne energie van lichamen niet afhankelijk is van de mechanische energie van het lichaam, maar van de temperatuur van het lichaam en de aggregatietoestand van de substantie. Met andere woorden: de interne energie van een lichaam wordt bepaald door de bewegingssnelheid van de deeltjes waaruit het lichaam bestaat en hun relatieve positie.
De volgende fase van het bestuderen van nieuw materiaal is het bestuderen van manieren om de interne energie van het lichaam te veranderen. Experimenten kunnen duidelijk aantonen dat de interne energie van een lichaam kan worden veranderd door arbeid te verrichten (aan het lichaam en het lichaam zelf) en door warmteoverdracht.
Dit zijn de volgende experimenten:
1. Interne energie veranderen door werk aan het lichaam te doen.
Ervaring nr. 2. Wrijf de munt over een houten liniaal, met de handpalmen tegen elkaar. Studenten concluderen: de interne energie van het lichaam is toegenomen.
Ervaring nr. 3. Neem een luchtvuursteentje. Bij snelle compressie wordt de lucht zo sterk opgewarmd dat de etherdamp die zich in de cilinder onder de zuiger bevindt, ontbrandt. Studenten concluderen: de interne energie van het lichaam is toegenomen.
2. Verandering in interne energie wanneer het lichaam zelf arbeid verricht.
Ervaring nr. 4. We pompen lucht in een dikwandig glazen vat, afgesloten met een stop, via een speciaal gat erin. Na enige tijd zal de kurk uit het vat vliegen. Op het moment dat de kurk uit het vat vliegt, is het noodzakelijk om de aandacht van de leerlingen te vestigen op de vorming van mist in het glazen vat, wat duidt op een verlaging van de temperatuur van de lucht en de waterdamp die zich daarin bevinden. Studenten concluderen: de interne energie van het lichaam is afgenomen.
3. Verandering in interne energie door warmteoverdracht.
Gebaseerd op ervaringen uit het dagelijks leven (een lepel gedoopt in hete thee warmt op, een uitgeschakeld heet strijkijzer in de kamer koelt af).
Op basis van alle voorbeelden en experimenten wordt een algemene conclusie getrokken: de interne energie van een lichaam kan in de loop van de tijd veranderen (toenemen of afnemen) tijdens de warmte-uitwisseling van een bepaald lichaam met de omringende lichamen en wanneer mechanisch werk wordt uitgevoerd (dia 9 ).
Dia 9
Bij het uitleggen van de mechanismen en methoden van warmteoverdracht is het noodzakelijk om de aandacht van leerlingen te vestigen op het feit dat warmteoverdracht altijd in een bepaalde richting plaatsvindt: van een lichaam met een hogere temperatuur naar een lichaam met een lagere temperatuur, wat er in wezen toe leidt dat leerlingen naar het idee van de tweede wet van de thermodynamica.
Dia 10
Overweging verschillende types Warmteoverdracht begint met thermische geleidbaarheid. Overweeg om dit fenomeen te bestuderen ervaring nr. 5 met verwarming van een metalen staaf (zie leerboek Peryshkin A.V. Physics-8) Op basis van de resultaten van het experiment stellen studenten het feit vast van warmteoverdracht van het ene deel van het lichaam naar het andere en leggen dit uit.
Vervolgens wordt het concept van goede en slechte warmtegeleiders geïntroduceerd. Demonstreer duidelijk op eenvoudig experimenten nr. 6, nr. 7, nr. 8 beschreef in het leerboek (A.V. Peryshkin Physics-8) de verschillende thermische geleidbaarheid van stoffen en beschouwt het gebruik in de technologie, het dagelijks leven en de aard van de eigenschappen van lichamen om warmte op een andere manier te geleiden (dia 11-13).
Dia 11
Dia 12
Dia 13
De studie van het fenomeen convectie begint met de volgende verklaring: ervaring nr. 9: een reageerbuis gevuld met water wordt verwarmd op een alcohollamp in het bovenste gedeelte van de reageerbuis. Tegelijkertijd blijft het water onderin de reageerbuis koud en kookt het bovenaan. Studenten concluderen dat water een slechte thermische geleidbaarheid heeft. Maar! Vraag voor studenten: Hoe wordt water verwarmd in bijvoorbeeld een waterkoker? Waarom?
We krijgen antwoorden op deze vragen als we het volgende doen ervaring nr. 10: We zullen een kolf met water van onderaf verwarmen op een alcohollamp, aan de onderkant bevindt zich een kristal van kaliumpermanganaat, dat de convectiestromen kleurt.
Om convectie in gassen aan te tonen, kun je een projector gebruiken en in de projectie op het scherm de convectiestromen van een brandende kaars observeren.
Als voorbeelden van convectie in de natuur wordt de vorming van dag- en nachtbries beschouwd, en in technologie - de vorming van trek in schoorstenen, convectie bij waterverwarming, waterkoeling van een verbrandingsmotor (dia 14-15).
Dia 14
Dia 15
Het concept van straling als een van de methoden voor warmteoverdracht kan beginnen door de vraag te stellen: “Kan de energie van de zon door thermische geleiding naar de aarde worden overgedragen? Convectie? Studenten concluderen dat dit niet mogelijk is en dat er daarom een andere manier is om warmte over te dragen.
U kunt uw kennismaking met straling voortzetten door te zetten experiment nr. 11 door een warmteontvanger te verwarmen die is aangesloten op een vloeistofdrukmeter en zich op enige afstand aan de zijkant van de elektrische kachel bevindt
Studenten krijgen de vraag voorgelegd: waarom wordt de lucht in de warmteontvanger warm? Warmtegeleiding en convectie zijn hier immers uitgesloten. Er doet zich een problematische situatie voor, als resultaat van de discussie waarvan studenten tot de conclusie komen dat er in dit geval een speciaal type transmissie is - straling - warmteoverdracht met behulp van onzichtbare stralen.
Volgende experiment nr. 12 Ontdek dat de lichamen met ander oppervlak hebben verschillende capaciteiten energie absorberen. Hiervoor gebruiken ze een koellichaam, waarvan er één een glanzend metalen oppervlak heeft, de andere is zwart en ruw.
Ter afsluiting van de uitleg kunnen we voorbeelden geven van straling in de natuur en technologie (dia 16-17).
Dia 16
Natuurkundeles in groep 8 over het onderwerp: "Interne energie. Manieren om interne energie te veranderen"
Lesdoelen:
- Vorming van het concept van “interne energie van het lichaam” gebaseerd op MCT van de structuur van materie.
- Kennismaking met manieren om de interne energie van het lichaam te veranderen.
- Vorming van het concept van "warmteoverdracht" en het vermogen om kennis van MCT van de structuur van materie toe te passen bij het verklaren van thermische verschijnselen.
- Het ontwikkelen van interesse in natuurkunde door middel van demonstratie interessante voorbeelden manifestaties van thermische verschijnselen in de natuur en technologie.
- Rechtvaardiging van de noodzaak om thermische verschijnselen te bestuderen om deze kennis in het dagelijks leven toe te passen.
- Ontwikkeling van informatie - communicatieve competenties studenten.
Lestype. Gecombineerde les.
Soort les. Les - presentatie
Lesformaat.
Interactief gesprek, demonstratie-experiment, verhaal, zelfstandig werkVormen van studentenwerk.
Teamwerk, individueel werk, werk in groepen.Apparatuur: elektronische presentatie “Interne energie. Methoden voor het veranderen van interne energie", computer, projector.
Tijdens de lessen
Tijd organiseren.
Goedemiddag Vandaag zullen we in de les kennis maken met een ander type energie, ontdekken waar het van afhangt en hoe het kan worden veranderd.Kennis actualiseren.
- Herhaling van basisbegrippen: energie, kinetische en potentiële energie, mechanische arbeid.
Nieuw materiaal leren.
Docent . Naast de hierboven genoemde concepten, moet er ook rekening mee worden gehouden dat er twee typen zijnmechanische energiekunnen in elkaar overgaan (overgaan), bijvoorbeeld wanneer een lichaam valt. Beschouw een vrij vallende bal. Het is duidelijk dat bij het vallen de hoogte boven het oppervlak afneemt en de snelheid toeneemt, dit betekent dat de potentiële energie afneemt en de kinetische energie toeneemt. Het moet duidelijk zijn dat deze twee processen niet afzonderlijk plaatsvinden, maar met elkaar verbonden zijn, en dat zeggen ze ookpotentiële energie verandert in kinetische energie.
Om te begrijpen wat de interne energie van een lichaam is, is het noodzakelijk om de volgende vraag te beantwoorden: waar zijn alle lichamen van gemaakt?
Studenten . Lichamen bestaan uit deeltjes die voortdurend chaotisch bewegen en met elkaar interageren.
Docent . En als ze bewegen en op elkaar inwerken, hebben ze kinetische en potentiële energie, die interne energie vormen.
Studenten. Het blijkt dat alle lichamen dezelfde interne energie hebben, wat betekent dat de temperatuur hetzelfde moet zijn. Maar dit is niet zo.
Docent. Natuurlijk niet. Lichamen hebben verschillende interne energieën, en we zullen proberen erachter te komen waar de interne energie van een lichaam van afhankelijk is en waar niet van afhangt.
Definitie.
Kinetische energie
deeltjesbewegingen enpotentiële energiehun interacties vormeninterne energie van het lichaam.Interne energie wordt aangegeven meten het wordt, net als alle andere soorten energie, gemeten in J (joule).
Daarom hebben we een formule voor de interne energie van het lichaam:. Waar onder verwijst naar de kinetische energie van lichaamsdeeltjes, en door– hun potentiële energie.
Laten we de vorige les herinneren, waarin we het hadden over het feit dat de beweging van deeltjes van een lichaam wordt gekenmerkt door de temperatuur ervan, aan de andere kant is de interne energie van het lichaam gerelateerd aan de aard (activiteit) van de beweging van deeltjes. Daarom zijn interne energie en temperatuur onderling verbonden concepten. Wanneer de lichaamstemperatuur stijgt, neemt ook de interne energie toe, en wanneer deze daalt, neemt deze af.
We ontdekten dat de interne energie van het lichaam kan veranderen. Laten we manieren overwegen om de interne energie van het lichaam te veranderen.
Je bent al bekend met het concept van mechanisch werk van een lichaam; het wordt geassocieerd met de beweging van een lichaam wanneer er een bepaalde kracht op wordt uitgeoefend. Als mechanisch werk wordt uitgevoerd, verandert de energie van het lichaam, en hetzelfde kan specifiek worden gezegd over de interne energie van het lichaam. Het is handig om dit in een diagram weer te geven:

Docent De methode om de interne energie van een lichaam door wrijving te vergroten is bij mensen al sinds de oudheid bekend. Dit is hoe mensen vuur maakten. Wat kun je bijvoorbeeld waarnemen als je in werkplaatsen werkt en onderdelen draait met een vijl? (Onderdelen werden heet). Als een persoon het koud heeft, begint hij onwillekeurig te huiveren. Waarom denk je dat? (Bij trillen treden spiersamentrekkingen op. Door spierwerk neemt de interne energie van het lichaam toe en wordt het warmer). Welke conclusie kan worden getrokken uit wat er is gezegd?
Studenten . De interne energie van een lichaam verandert wanneer er gewerkt wordt. Als het lichaam zelf wel werkt, neemt de interne energie af, en als er aan wordt gewerkt, neemt de interne energie toe.
Docent . In de technologie, de industrie en de dagelijkse praktijk komen we voortdurend veranderingen tegen in de interne energie van een lichaam tijdens het uitvoeren van werk: verwarming van lichamen tijdens het smeden, tijdens impact; het uitvoeren van werkzaamheden met perslucht of stoom.
Laten we een beetje ontspannen en tegelijkertijd wat ontdekken Interessante feiten uit de geschiedenis van thermische verschijnselen (twee studenten geven vooraf voorbereide korte berichten).
Bericht 1. Hoe wonderen werden verricht.
De oude Griekse monteur Heron van Alexandrië, de uitvinder van de fontein die zijn naam draagt, heeft ons een beschrijving nagelaten van twee ingenieuze manieren waarop de Egyptische priesters het volk misleidden om in wonderen te geloven.
In Figuur 1 zie je een hol metalen altaar, met daaronder een mechanisme verborgen in de kerker dat de deuren van de tempel beweegt. Het altaar stond erbuiten. Wanneer er een vuur wordt aangestoken, oefent de lucht in het altaar, als gevolg van de verwarming, meer druk uit op het water in het vat dat onder de vloer verborgen is; Vanuit het vat wordt water door een buis naar buiten geperst en in een emmer gegoten, die, wanneer hij wordt neergelaten, een mechanisme activeert dat de deuren draait (Fig. 2). Verbaasde toeschouwers, zich niet bewust van de onder de vloer verborgen installatie, zien een ‘wonder’ voor zich: zodra het vuur op het altaar laait, lossen de deuren van de tempel, ‘luisterend naar de gebeden van de priester’, op terwijl als het op zichzelf...

Het ‘wonder’ van de Egyptische priesters blootleggen: de deuren van de tempel worden geopend door de werking van offervuur.
Bericht 2. Hoe wonderen werden verricht.
Een ander denkbeeldig wonder dat door de priesters werd verricht, wordt getoond in Fig. 3. Wanneer een vlam op het altaar brandt, verwijdert de lucht, die uitzet, olie uit het onderste reservoir in de buizen die verborgen zijn in de figuren van de priesters, en dan wordt de olie op wonderbaarlijke wijze zelf aan het vuur toegevoegd... Maar zodra de priester die de leiding had over dit altaar verwijderde stilletjes de plug uit het dekselreservoir - en het uitstromen van olie stopte (omdat overtollige lucht vrijelijk door het gat ontsnapte); De priesters namen hun toevlucht tot deze truc toen de offers van de aanbidders te mager waren.
Docent. Hoe bekend zijn we allemaal met ochtendthee! Het is zo lekker om thee te zetten, suiker in een kopje te gieten en een beetje te drinken, met een kleine lepel. Slechts één ding is slecht: de lepel is te heet! Wat is er met de lepel gebeurd? Waarom steeg haar temperatuur? Waarom nam haar interne energie toe? Hebben wij daaraan gewerkt?
Studenten . Nee, dat deden ze niet.
Docent . Laten we eens kijken waarom de verandering in interne energie plaatsvond.
Aanvankelijk is de temperatuur van het water hoger dan de temperatuur van de lepel, en daarom is de snelheid van de watermoleculen groter. Dit betekent dat watermoleculen meer kinetische energie hebben dan de deeltjes van het metaal waaruit de lepel is gemaakt. Wanneer ze botsen met metaaldeeltjes, dragen watermoleculen een deel van hun energie over, en neemt de kinetische energie van de metaaldeeltjes toe, en neemt de kinetische energie van watermoleculen af. Deze methode om de interne energie van lichamen te veranderen wordt genoemd warmteoverdracht . In ons dagelijks leven komen we dit fenomeen vaak tegen. In water, wanneer u op de grond of in de sneeuw ligt, koelt het lichaam bijvoorbeeld af, wat kan leiden tot verkoudheid of bevriezing. Bij strenge vorst klimmen eenden graag het water in. Waarom denk je dat? (Bij strenge vorst is de watertemperatuur aanzienlijk hoger dan de omgevingsluchttemperatuur, waardoor de vogel in water minder afkoelt dan in lucht). Warmteoverdracht vindt op verschillende manieren plaats, maar hierover zullen we in de volgende les praten.
Er zijn dus twee mogelijke manieren om de interne energie te veranderen. Welke?
Studenten . Werkprestaties en warmteoverdracht.
Consolidatie van het bestudeerde materiaal.Laten we nu eens kijken hoe goed je hebt geleerd nieuw materiaal de les van vandaag. Ik zal vragen stellen en jij zult proberen ze te beantwoorden.
Vraag 1 . Gegoten in één glas koud water, in de andere - dezelfde hoeveelheid kokend water. In welk glas heeft het water meer interne energie? (In de tweede, omdat de temperatuur hoger is).
Vraag 2. Twee koperen staven hebben dezelfde temperatuur, maar de massa van de ene is 1 kg en de andere is 0,5 kg. Welke van de twee gegeven staven heeft een grotere interne energie? (De eerste, omdat de massa groter is).
Vraag 3. De hamer wordt heet als hij bijvoorbeeld op een aambeeld wordt geslagen en als hij op een warme zomerdag in de zon ligt. Noem manieren om in beide gevallen de interne energie van de hamer te veranderen. (In het eerste geval wordt er gewerkt en in het tweede geval warmteoverdracht).
Vraag 4 . Water wordt in een metalen mok gegoten. Welke van de volgende oorzaken veroorzaakt een verandering in de interne energie van water? (13)
- Water verwarmen op een hete kachel.
- Het uitvoeren van werkzaamheden op het water, het binnenbrengen ervan voorwaartse beweging samen met de mok.
- Voer werkzaamheden aan water uit door het met een mixer te mengen.
Docent . En nu stel ik voor dat je voor jezelf gaat werken. (De leerlingen worden in 6 groepen verdeeld en er wordt in groepen verder gewerkt). Voor je ligt een vel papier met drie taken.
Oefening 1. Wat veroorzaakt de verandering in de interne energie van lichamen in de volgende verschijnselen:
- water verwarmen met een boiler;
- het koelen van voedsel dat in de koelkast is geplaatst;
- het ontsteken van een lucifer wanneer deze tegen een doos wordt geslagen;
- sterke verwarming en verbranding kunstmatige satellieten aarde wanneer ze de lagere dichte lagen van de atmosfeer binnendringen;
- als je de draad snel op dezelfde plek buigt, eerst in de ene richting en dan in de andere, dan wordt deze plek erg heet;
- eten koken;
- Als je snel langs een paal of touw naar beneden glijdt, kun je je handen verbranden;
- het verwarmen van het zwembadwater op een warme zomerdag;
- Bij het inslaan van een spijker warmt de kop op;
- Een lucifer laait op als deze in een kaarsvlam wordt geplaatst.
Voor twee groepen – met wrijving; de andere twee groepen - tijdens impact en nog twee groepen - tijdens compressie.
Reflectie.
- Welke nieuwe of interessante dingen heb je vandaag in de klas geleerd?
- Hoe heb je de stof geleerd die je hebt behandeld?
- Wat waren de moeilijkheden? Ben je erin geslaagd ze te overwinnen?
- Zal de kennis die u in de les van vandaag heeft opgedaan nuttig voor u zijn?
De les samenvattend.Vandaag maakten we kennis met de basisconcepten van de sectie “Thermische verschijnselen”: interne energie en warmteoverdracht en raakten we vertrouwd met de manieren om de interne energie van lichamen te veranderen. De opgedane kennis helpt je bij het verklaren en voorspellen van het verloop van thermische processen die je in je leven tegenkomt.
Huiswerk. § 2, 3. Experimentele taken:
- Gebruik een huisthermometer om de temperatuur te meten van het water dat in een pot of fles wordt gegoten.
Sluit het vat goed en schud het krachtig gedurende 10-15 minuten. Meet vervolgens de temperatuur opnieuw.
Om warmteoverdracht van uw handen te voorkomen, draagt u wanten of wikkelt u het vat in een handdoek.
Welke methode voor het veranderen van de interne energie heb je gebruikt? Uitleggen. - Neem een elastiekje dat met een ring vastgebonden is, breng het bandje op je voorhoofd aan en noteer de temperatuur ervan. Houd het rubber met uw vingers vast, rek het meerdere keren krachtig uit en druk het, wanneer het uitgerekt is, opnieuw tegen uw voorhoofd. Trek een conclusie over de temperatuur en de redenen die de verandering hebben veroorzaakt.
Voorbeeld:
Om presentatievoorbeelden te gebruiken, maakt u een account voor uzelf aan ( rekening) Google en log in:
Onderwerpen van de Unified State Examination-codifier: interne energie, warmteoverdracht, soorten warmteoverdracht.
Deeltjes van elk lichaam – atomen of moleculen – voeren een chaotische continue beweging uit (de zogenaamde thermische beweging ). Daarom heeft elk deeltje een bepaalde kinetische energie.
Bovendien interageren materiedeeltjes met elkaar door krachten van elektrische aantrekking en afstoting, maar ook door nucleaire krachten. Daarom heeft het hele systeem van deeltjes van een bepaald lichaam ook potentiële energie.
De kinetische energie van thermische beweging van deeltjes en de potentiële energie van hun interactie vormen zich samen de nieuwe soort energie, die niet wordt gereduceerd tot de mechanische energie van het lichaam (dat wil zeggen de kinetische energie van de beweging van het lichaam als geheel en de potentiële energie van de interactie met andere lichamen). Dit type energie wordt interne energie genoemd.
De interne energie van een lichaam is de totale kinetische energie van de thermische beweging van zijn deeltjes plus de potentiële energie van hun interactie met elkaar.
De interne energie van een thermodynamisch systeem is de som van de interne energieën van de lichamen die deel uitmaken van het systeem.
De interne energie van het lichaam wordt dus gevormd door de volgende termen.
1. Kinetische energie van continue chaotische beweging van lichaamsdeeltjes.
2. Potentiële energie van moleculen (atomen), veroorzaakt door de krachten van intermoleculaire interactie.
3. Energie van elektronen in atomen.
4. Intranucleaire energie.
Wanneer het eenvoudigste model stoffen - Ideaal gas- er kan een expliciete formule worden verkregen voor interne energie.
Interne energie van een monatomisch ideaal gas
De potentiële energie van interactie tussen deeltjes van een ideaal gas is nul (bedenk dat we in het ideale gasmodel de interactie van deeltjes op afstand verwaarlozen). Daarom wordt de interne energie van een monatomisch ideaal gas gereduceerd tot de totale kinetische energie van de translationele (voor een polyatomisch gas moet men ook rekening houden met de rotatie van moleculen en trillingen van atomen binnen moleculen) beweging van zijn atomen. Deze energie kan worden gevonden door het aantal gasatomen te vermenigvuldigen met de gemiddelde kinetische energie van één atoom:
We zien dat de interne energie van een ideaal gas (massa en chemische samenstelling die onveranderd zijn) is alleen een functie van de temperatuur. In een echt gas, vloeibaar of vast, zal de interne energie ook afhangen van het volume - wanneer het volume verandert, verandert immers de relatieve rangschikking van de deeltjes en, als gevolg daarvan, de potentiële energie van hun interactie.
Statusfunctie
De belangrijkste eigenschap van interne energie is dat dit zo is staatfunctie thermodynamisch systeem. De interne energie wordt namelijk op unieke wijze bepaald door een reeks macroscopische parameters die het systeem karakteriseren, en is niet afhankelijk van de ‘prehistorie’ van het systeem, d.w.z. over de toestand waarin het systeem zich voorheen bevond en hoe het specifiek in deze toestand terechtkwam.
Wanneer een systeem dus van de ene toestand naar de andere overgaat, wordt de verandering in zijn interne energie alleen bepaald door de begin- en eindtoestand van het systeem en hangt niet af van het pad van de overgang van de begintoestand naar de eindtoestand. Als het systeem terugkeert naar zijn oorspronkelijke staat, is de verandering in zijn interne energie nul.
De ervaring leert dat er slechts twee manieren zijn om de interne energie van een lichaam te veranderen:
Het uitvoeren van mechanische werkzaamheden;
warmteoverdracht.
Simpel gezegd: met slechts twee stuks kun je een waterkoker opwarmen verschillende manieren: wrijf het ergens mee of steek het in brand :-) Laten we deze methoden in meer detail bekijken.
Verandering in interne energie: werk gedaan
Als het werk klaar is boven lichaam, dan neemt de interne energie van het lichaam toe.
Nadat je er bijvoorbeeld met een hamer op hebt geslagen, warmt een spijker op en raakt hij licht vervormd. Maar temperatuur is een maatstaf voor de gemiddelde kinetische energie van deeltjes in een lichaam. Het verwarmen van een spijker duidt op een toename van de kinetische energie van de deeltjes: in feite worden de deeltjes versneld door de impact van een hamer en door de wrijving van de spijker op de plaat.
Vervorming is niets meer dan de verplaatsing van deeltjes ten opzichte van elkaar; Na een botsing ondergaat een nagel drukvervorming, komen de deeltjes dichter bij elkaar, nemen de afstotende krachten daartussen toe, en dit leidt tot een toename van de potentiële energie van de nageldeeltjes.
De interne energie van de nagel is dus toegenomen. Dit was het resultaat van het werk dat eraan werd gedaan: het werk werd gedaan door de hamer en de wrijvingskracht op het bord.
Als het werk klaar is onszelf lichaam, dan neemt de interne energie van het lichaam af.
Laat bijvoorbeeld perslucht in een thermisch geïsoleerd vat onder een zuiger uitzetten en een bepaalde last optillen, waardoor arbeid wordt verricht (het proces in een thermisch geïsoleerd vat heet adiabatisch. We zullen het adiabatische proces bestuderen door de eerste wet van de thermodynamica te beschouwen). Tijdens dit proces zal de lucht afkoelen - de moleculen die achter de bewegende zuiger slaan, geven hem een deel van hun kinetische energie. (Op dezelfde manier maakt een voetballer, die een snel vliegende bal met zijn voet tegenhoudt, er een beweging mee van bal en dempt zijn snelheid.) Daarom neemt de interne energie van de lucht af.
De lucht werkt dus ten koste van zijn interne energie: aangezien het vat thermisch geïsoleerd is, is er geen energiestroom naar de lucht vanuit externe bronnen, en kan de lucht alleen energie onttrekken om werk te doen uit zijn eigen reserves. .
Verandering in interne energie: warmteoverdracht
Warmteoverdracht is het proces waarbij interne energie wordt overgedragen van een heter lichaam naar een kouder lichaam, niet geassocieerd met de uitvoering van mechanisch werk. Warmteoverdracht kan plaatsvinden via direct contact van lichamen, of via een tussenmedium (en zelfs via een vacuüm). Warmteoverdracht wordt ook wel genoemd warmte uitwisseling.
Er zijn drie soorten warmteoverdracht: geleiding, convectie en thermische straling.
Nu zullen we ze in meer detail bekijken.
Warmtegeleiding
Als je het ene uiteinde van een ijzeren staaf in het vuur steekt, zul je hem, zoals we weten, niet lang in je hand houden. Het gebied betreden hoge temperatuur beginnen ijzeratomen intenser te trillen (d.w.z. ze verwerven extra kinetische energie) en veroorzaken meer sterke slagen door hun buren.
De kinetische energie van naburige atomen neemt ook toe, en nu geven deze atomen extra kinetische energie aan hun buren. Dus van sectie tot sectie verspreidt de hitte zich geleidelijk langs de staaf - vanaf het uiteinde dat in het vuur is geplaatst tot aan onze hand. Dit is de thermische geleidbaarheid (Fig. 1) (Afbeelding van Educationalelectronicsusa.com).

Rijst. 1. Thermische geleidbaarheid
Thermische geleidbaarheid is de overdracht van interne energie van meer verwarmde delen van het lichaam naar minder verwarmde delen als gevolg van thermische beweging en interactie van lichaamsdeeltjes.
Warmtegeleiding verschillende stoffen verschillend. Metalen hebben een hoge thermische geleidbaarheid: de beste warmtegeleiders zijn zilver, koper en goud. De thermische geleidbaarheid van vloeistoffen is veel minder. Gassen geleiden warmte zo slecht dat ze als warmte-isolatoren worden beschouwd: gasmoleculen hebben vanwege de grote afstanden tussen hen een zwakke wisselwerking met elkaar. Daarom hebben ramen bijvoorbeeld dubbele kozijnen: een luchtlaag voorkomt dat warmte ontsnapt).
Daarom zijn poreuze lichamen zoals baksteen, watten of bont slechte warmtegeleiders. Ze bevatten lucht in hun poriën. Geen wonder bakstenen huizen worden als de warmste beschouwd, en bij koud weer dragen mensen bontjassen en jassen met een laag dons of polyestervulling.
Maar als de lucht de warmte zo slecht geleidt, waarom warmt de kamer dan op door de radiator?
Dit gebeurt als gevolg van een ander type warmteoverdracht: convectie.
Convectie
Convectie is de overdracht van interne energie in vloeistoffen of gassen als gevolg van de circulatie van stromen en het mengen van materie.
De lucht nabij de batterij warmt op en zet uit. De zwaartekracht die op deze lucht inwerkt blijft hetzelfde, maar de opwaartse kracht van de omringende lucht neemt toe, waardoor de verwarmde lucht naar het plafond begint te zweven. In de plaats komt koude lucht(hetzelfde proces, maar op veel grotere schaal, vindt voortdurend plaats in de natuur: zo ontstaat de wind), waarmee hetzelfde wordt herhaald.
Als gevolg hiervan ontstaat luchtcirculatie, die als voorbeeld van convectie dient: de verspreiding van warmte in de kamer wordt uitgevoerd door luchtstromen.
Een volledig soortgelijk proces kan worden waargenomen in vloeistoffen. Wanneer u een ketel of pan met water op het fornuis zet, wordt het water voornamelijk verwarmd door convectie (de bijdrage aan de thermische geleidbaarheid van water is zeer onbeduidend).
Convectiestromen in lucht en vloeistof worden getoond in Fig. 2 (afbeeldingen van Physics.arizona.edu).
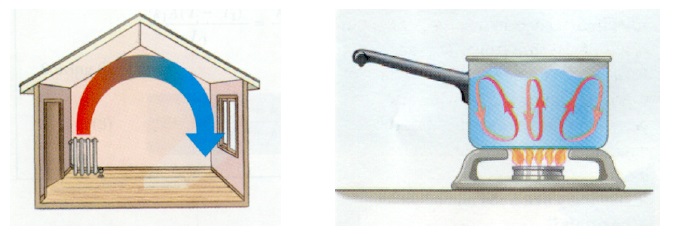
Rijst. 2. Convectie
IN vaste stoffen er is geen convectie: deeltjesinteractiekrachten zijn groot, deeltjes oscilleren nabij vaste ruimtelijke punten (knooppunten) kristal rooster), en onder dergelijke omstandigheden kunnen zich geen materiestromen vormen.
Voor de circulatie van convectiestromen bij het verwarmen van een kamer is het noodzakelijk dat de verwarmde lucht wordt verwarmd er was ruimte om naar voren te komen. Als de radiator onder het plafond wordt geïnstalleerd, zal er geen circulatie plaatsvinden - warme lucht onder het plafond zal dat zo blijven. Daarom worden er verwarmingstoestellen geplaatst aan de onderkant kamers. Om dezelfde reden wordt de ketel aangezet op vuur, waardoor de verwarmde waterlagen, die opstijgen, plaats maken voor koudere.
Integendeel, de airconditioner moet zo hoog mogelijk worden geplaatst: dan begint de gekoelde lucht te dalen en komt warmere lucht in de plaats. Bij het verwarmen van de kamer zal de circulatie in de tegenovergestelde richting gaan ten opzichte van de stromingsbeweging.
Thermische straling
Hoe ontvangt de aarde energie van de zon? Warmtegeleiding en convectie zijn uitgesloten: we zijn gescheiden door 150 miljoen kilometer luchtloze ruimte.
Het derde type warmteoverdracht werkt hier: thermische straling. Straling kan zich zowel in de materie als in het vacuüm voortplanten. Hoe ontstaat het?
Het blijkt dat elektrisch en magnetisch veld Ze zijn nauw verwant aan elkaar en hebben één opmerkelijke eigenschap. Als elektrisch veld verandert met de tijd, dan genereert het een magnetisch veld, dat over het algemeen ook met de tijd verandert (dit wordt uitgebreider besproken in de folder over elektromagnetische inductie). Op zijn beurt genereert een magnetisch wisselveld een elektrisch wisselveld, dat weer een magnetisch wisselveld genereert, dat weer een elektrisch wisselveld genereert...
Als resultaat van de ontwikkeling van dit proces, elektromagnetische golf- elektrische en magnetische velden ‘ingrijpen’ met elkaar. Net als het geluid elektromagnetische golven hebben een voortplantingssnelheid en -frequentie - in dit geval is dit de frequentie waarmee de grootte en richting van de velden in de golf fluctueren. Zichtbaar licht - speciaal geval elektromagnetische golven.
De voortplantingssnelheid van elektromagnetische golven in een vacuüm is enorm: km/s. Licht reist dus in iets meer dan een seconde van de aarde naar de maan.
Het frequentiebereik van elektromagnetische golven is zeer breed. We zullen meer vertellen over de omvang van elektromagnetische golven in de bijbehorende folder. Hier merken we alleen op dat zichtbaar licht slechts een klein bereik van deze schaal is. Daaronder bevinden zich de frequenties van infraroodstraling, daarboven bevinden zich de frequenties van ultraviolette straling.
Bedenk nu dat atomen, hoewel ze over het algemeen elektrisch neutraal zijn, positief geladen protonen en negatief geladen elektronen bevatten. Deze geladen deeltjes, die samen met atomen chaotische bewegingen uitvoeren, creëren wisselende elektrische velden en zenden daardoor elektromagnetische golven uit. Deze golven worden genoemd thermische straling- als herinnering dat hun bron de thermische beweging van materiedeeltjes is.
De bron van thermische straling is elk lichaam. In dit geval voert de straling een deel van de interne energie weg. Nadat ze de atomen van een ander lichaam hebben ontmoet, versnelt de straling ze met haar oscillatie elektrisch veld, en de interne energie van dit lichaam neemt toe. Zo genieten we van de zonnestralen.
Bij normale temperaturen liggen de frequenties van thermische straling in het infrarode bereik, zodat het oog dit niet waarneemt (we zien niet hoe we “gloeien”). Wanneer een lichaam opwarmt, beginnen de atomen golven met hogere frequenties uit te zenden. Een ijzeren spijker kan roodgloeiend worden verwarmd - tot een zodanige temperatuur worden gebracht dat de thermische straling het onderste (rode) deel van het zichtbare bereik bereikt. En de zon lijkt ons geelwit: de temperatuur op het oppervlak van de zon is zo hoog dat het stralingsspectrum alle frequenties van zichtbaar licht bevat, en zelfs ultraviolet, waardoor we bruin worden.
Laten we nog eens kijken naar de drie soorten warmteoverdracht (Figuur 3) (afbeeldingen van beodom.com).

Rijst. 3. Drie soorten warmteoverdracht: geleiding, convectie en straling